Cierres Defectos Septales
CeraFlex
Balón de medición de defectos cardíacos para realizar procedimientos de cierre percutáneo
Disclaimer: "Cierres de Defectos Septales Ceraflex" is a trademark of Lifetech Scientific (Shenzhen) Co., Ltd. ("Lifetech "). SMT Iberia is the authorised distributor of Lifetech for Spain. Descargo de responsabilidad: "Cierres de Defectos Septales Ceraflex" es una marca comercial de Lifetech Scientific (Shenzhen) Co., Ltd. ("Lifetech"). SMT Iberia es el distribuidor autorizado de Lifetech para España.
CARACTERÍSTICAS TÉCNICAS
Sistema de Entrega Innovador
Rotación flexible de 360°, flexible, posicionamiento preciso.
Sistema de entrega con prótesis premontada, para mayor comodidad.
Mango ergonómico con botón de seguridad para un desbloqueo controlado
Sistema CeraFlex
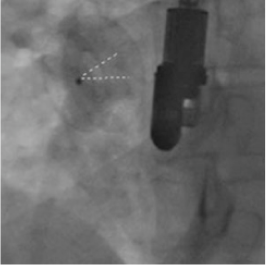
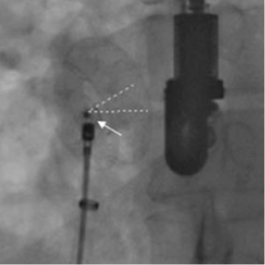
M.A. Astarcioglu, etc., Ceraflex versus Amplatzer occluder for secundum atrial septal defect closure, Multicenter clinical experience, Herz. 2015 Apr;40(Supplement 2):146-150. Epub 2015 Feb 8.
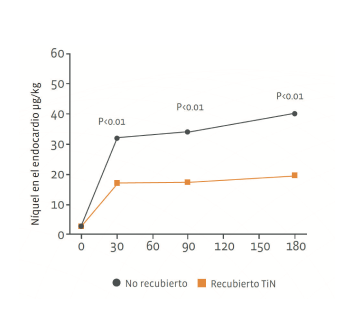
Revestimiento
de Nitruro de Titanio
Evita la liberación del Níquel.
Acelera la endotelización y cierra el defecto rápidamente.
Ablandanda el material de nitinol y proporciona un implante más adaptable y flexible.
Selección Estratégica de Membranas
Membrana de PTFE embebida en los dispositivos PDA para disminuir la derivación residual.
Membrana de PET en los dispositivos ASD/PFO para obtener una vaina de perfil más bajo.
Excelente
Estructura Trenzada
Ofrece beneficios potenciales al disminuir la posibilidad de formación de trombos en el disco auricular izquierdo con tecnología de mallado en lugar de abrazadera distal.
Ofrece una mejor adaptación en el tabique interauricular con disco flexible.
INFORMACIÓN TÉCNICA
Dispositivo de cierre de
defectos congénitos Ceraflex
Resonancia magnética (RM)
Un paciente después de haber recibido implante con el oclusor ASD es seguro para someterse a un procedimiento de resonancia magnética en las siguientes condiciones:
* Campo magnético estático de 3,0 Tesla o inferior
* Campo de gradiente espacial de ≤680 Gauss/cm
* Tasa máxima de absorción específica (SAR) promediada para todo el cuerpo de 2 W/kg durante 15 minutos de exploración
Vida útil esperada del dispositivo oclusor
El ASD Occluder es un dispositivo implantado permanentemente. En circunstancias normales, permanecerá en el cuerpo del paciente de por vida, a menos que el juicio profesional del médico requiera que se elimine.
Material/Sustancias en contacto con el paciente
Los implantes de oclusores están compuestos por
* NiTi (80 %-95 %), acero inoxidable (2 %-20 %), PA (0,1 %-0,8 %), PET (1,2 %-8,9 %) en oclusión HeartR ASDr
NiTi (80 %-95 %), TiN (~0 %), acero inoxidable (2 %-20 %), PA (0,1 %-0,8 %) y PET (1,2 %-8,9 %) en el oclusor Cera ASD
* NiTi (85 %-98 %), TiN (~0 %), PA (0,2 %-1 %), PET (2 %-15 %) en el oclusor Ceraflex ASD.
Seguimiento
Es importante programar visitas regulares de seguimiento. La visita de seguimiento debe realizarse a las 24 horas, 1, 3, 6 y 12 meses después del procedimiento y puede ser ajustada dependiendo de la condición del paciente.
ESPECIFICACIONES DE PRODUCTO
TIPOS DE COMUNICACIÓN INTERAURICULAR
- ASD
- ASD MULTIFENESTRADO
- FOP
- PDA


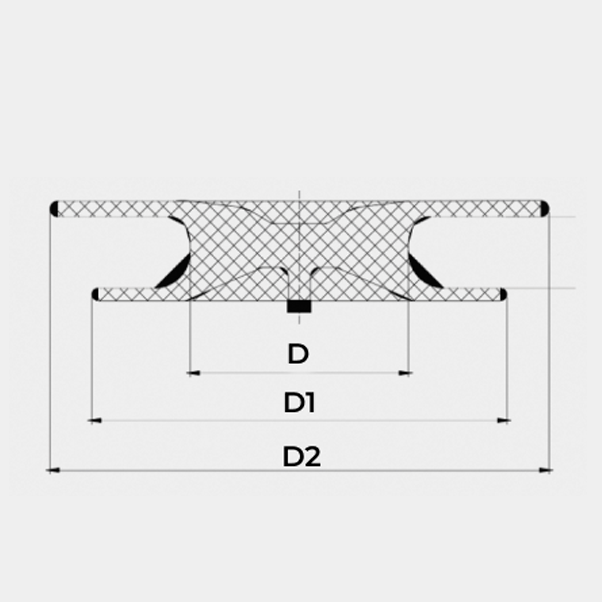
MEDIDAS Y REFERENCIAS
| REFERENCIA | D DIAMETRO CINTURA (MM) | D1 DIAMETRO DISCO DCHO (MM) | D2 DIAMETRO DISCO IZQ (MM) | L LONG CINTURA (MM) | TAMAÑO MÍNIMO DE LA VAINA | REFERENCIA DE LA VAINA |
|---|---|---|---|---|---|---|
| LT-ASDf-06 | 6 | 14 | 18 | 4 | 8 FR | SFA8F-f |
| LT-ASDf-08 | 8 | 16 | 20 | 4 | 8 FR | SFA8F-f |
| LT-ASDf-10 | 10 | 18 | 22 | 4 | 8 FR | SFA8F-f |
| LT-ASDf-12 | 12 | 22 | 26 | 4 | 9 FR | SFA9F-f |
| LT-ASDf-14 | 14 | 24 | 28 | 4 | 10 FR | SFA10F-f |
| LT-ASDf-16 | 16 | 26 | 30 | 4 | 10 FR | SFA10F-f |
| LT-ASDf-18 | 18 | 28 | 32 | 4 | 10 FR | SFA10F-f |
| LT-ASDf-20 | 20 | 30 | 34 | 4 | 12 FR | SFA12F-f |
| LT-ASDf-22 | 22 | 32 | 36 | 4 | 12 FR | SFA12F-f |
| LT-ASDf-24 | 24 | 34 | 38 | 4 | 12 FR | SFA12F-f |
| LT-ASDf-26 | 26 | 36 | 40 | 4 | 12 FR | SFA12F-f |
| LT-ASDf-28 | 28 | 38 | 42 | 4 | 12 FR | SFA12F-f |
| LT-ASDf-30 | 30 | 40 | 44 | 4 | 14 FR | SFA14F-f |
| LT-ASDf-32 | 32 | 42 | 46 | 4 | 14 FR | SFA14F-f |

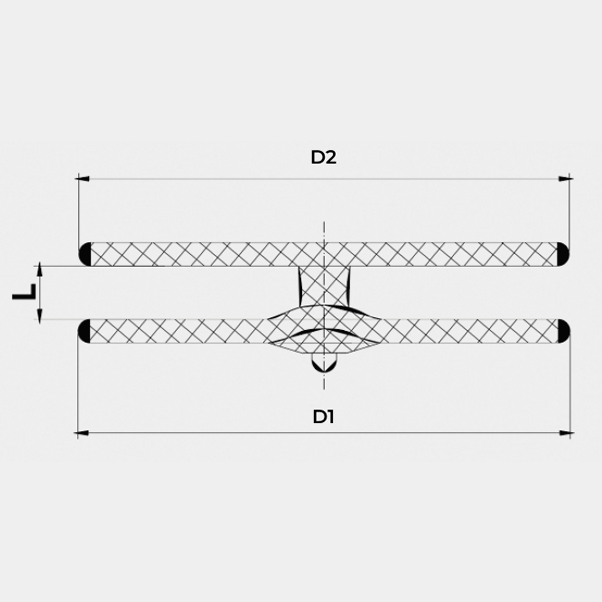
MEDIDAS Y REFERENCIAS
| REFERENCIA | D1 DIAMETRO DISCO DCHO (MM) | D2 DIAMETRO DISCO IZQ (MM) | L LONG CINTURA (MM) | TAMAÑO MÍNIMO DE LA VAINA | REFERENCIA DE LA VAINA |
|---|---|---|---|---|---|
| LT-ASDf-MF-1818 | 18 | 18 | 3 | 9 FR | SFA9F-f |
| LT-ASDf-MF-2525 | 25 | 25 | 3 | 10 FR | SFA10F-f |
| LT-ASDf-MF-3030 | 30 | 30 | 3 | 12 FR | SFA12F-f |
| LT-ASDf-MF-3535 | 35 | 35 | 3 | 14 FR | SFA14F-f |
| LT-ASDf-MF-4040 | 40 | 40 | 3 | 14 FR | SFA14F-f |

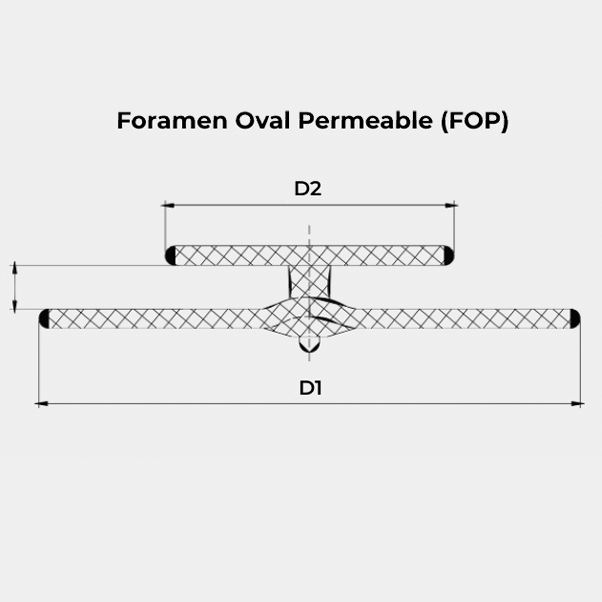
MEDIDAS Y REFERENCIAS
| REFERENCIA | D1 DIAMETRO DISCO DCHO (MM) | D2 DIAMETRO DISCO IZQ (MM) | L LONG CINTURA (MM) | TAMAÑO MÍNIMO DE LA VAINA | REFERENCIA DE LA VAINA |
|---|---|---|---|---|---|
| LT-PFOf-1818 | 18 | 18 | 3 | 9 FR | SFA9F-f |
| LT-PFOf-2518 | 25 | 18 | 3 | 10 FR | SFA10F-f |
| LT-PFOf-2525 | 25 | 25 | 3 | 10 FR | SFA10F-f |
| LT-PFOf-3025 | 30 | 25 | 3 | 12 FR | SFA12F-f |
| LT-PFOf-3030 | 30 | 30 | 3 | 12 FR | SFA12F-f |
| LT-PFOf-3525 | 35 | 25 | 3 | 14 FR | SFA14F-f |
MATERIAL Y COMPOSICIÓN
Composición del material del Oclusor CeraFlex FOP
| Descripción del Material | Sustancias en el Material | Concentración Porcentual (% w/w) |
|---|---|---|
| Malla / Punta | Nickel | >30 |
| Malla / Punta | Titanium | >30 |
| Malla / Punta | Cobalt | <1 |
| Malla / Punta | Iron | <1 |
| Malla / Punta | Carbon | <1 |
| Malla / Punta | Oxygen | <1 |
| Malla / Punta | Niobium | <1 |
| Malla / Punta | Copper | <1 |
| Malla / Punta | Chromium | <1 |
| Malla / Punta | Hydrogen | <1 |
| Malla / Punta | Nitrogen | <1 |
| Sutura | PA | <1 |
| Membrana | PET | 1 - 5 |
| Membrana | Binder Resin | <1 |
| Recubrimiento | Nitrogen | <1 |
| Recubrimiento | Titanium | <1 |

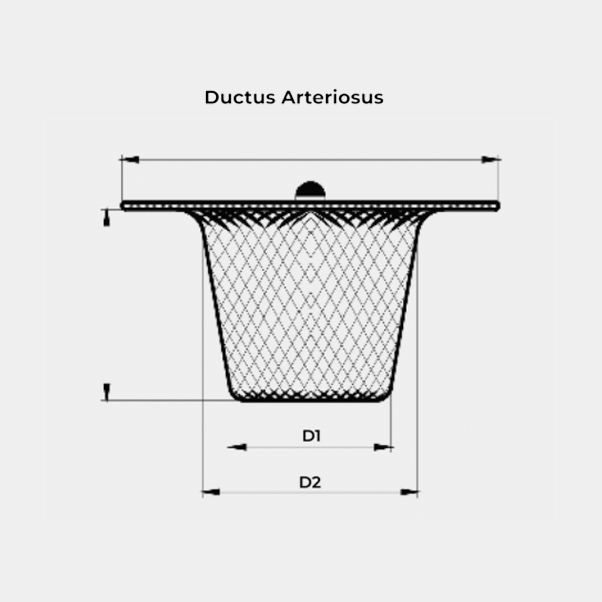
MEDIDAS Y REFERENCIAS
| REFERENCIA | FALDA DE RETENCIÓN | D1 DIAMETRO PROXIMAL (MM) | D2 DIAMETRO DISTAL (MM) | L LONG CINTURA (MM) | TAMAÑO MÍNIMO DE LA VAINA | REFERENCIA DE LA VAINA |
|---|---|---|---|---|---|---|
| LT-PDAf-0406 | 10 | 4 | 6 | 7 | 6 FR | SFP6F-f |
| LT-PDAf-0608 | 12 | 6 | 8 | 7 | 7 FR | SFP7F-f |
| LT-PDAf-0810 | 14 | 8 | 10 | 7 | 7 FR | SFP7F-f |
| LT-PDAf-1012 | 16 | 10 | 12 | 7 | 7 FR | SFP7F-f |
| LT-PDAf-1214 | 20 | 12 | 14 | 7 | 7 FR | SFP7F-f |
| LT-PDAf-1416 | 22 | 14 | 16 | 8 | 8 FR | SFP8F-f |
| LT-PDAf-1618 | 24 | 16 | 18 | 8 | 8 FR | SFP8F-f |
| LT-PDAf-1820 | 26 | 18 | 20 | 9 | 9 FR | SFP9F-f |
| LT-PDAf-2022 | 28 | 20 | 22 | 9 | 9 FR | SFP9F-f |
| LT-PDAf-2224 | 30 | 22 | 24 | 10 | 10 FR | SFP10F-f |